讀者:劉承恩
第二型糖尿病藥物治療建議
糖尿病的治療,首重衛教健康的生活型態、糖尿病自我照護與支持。藥物治療需要以病人為中心、考量併發症與不同治療目標。
成人第二型糖尿病合併確診或高風險之動脈粥樣硬化性心血管疾病 (atherosclerotic cardiovascular disease, ASCVD)、心衰竭 (heart failure, HF)、慢性腎臟病 (chronic kidney disease, CKD)需使用可以降低心臟、腎臟風險的藥物。
降低心臟、腎臟風險的藥物包含葡萄糖協同轉運蛋白2抑制劑 (Sodium glucose cotransporter 2 inhibitor, SGLT2i)和第一型升糖素類似胜肽受體促效劑 (Glucagon-like peptide 1 receptor agonists, GLP-1RA)建議於上述患者優先使用。
為了有效達到血糖目標,Metformin和相關複方藥物若無禁忌症或不耐受應該優先考慮。部分患者可以考慮起始複方藥物治療,可以延長治療失敗以致需要使用胰島素的時間。
除了強調血糖控制,體重控制也同樣重要,可以使用GLP-1RA達到血糖與體重控制目標。
藥物的使用需要以病人為中心來考量,包含評估心血管與腎臟疾病、藥物效果、低血糖風險、對體重的影響、健保規範與藥費、副作用與病人偏好。建議每3~6個月評估治療成效並調整藥物選擇。
若要使用針劑,建議優先使用GLP-1RA。有高血糖症狀(多吃、多喝、多尿、體重減輕)、HbA1c>10%或血糖≥300毫克/dL建議先使用胰島素 (Insulin)治療。使用胰島素後,除非有禁忌症或無法耐受,應該繼續使用Metformin。
需要避免基礎胰島素過量 (overbasalization)症狀,包括基礎胰島素超過0.5U/公斤/天、空腹飯後血糖差距大、低血糖、血糖波動大。
第二型糖尿病治療目標1:降低心臟腎臟風險
除了生活型態改善、飲食運動衛教之外,糖尿病的治療首重在高風險患者減少其心臟與腎臟風險。除了標準血壓、血脂、抗血栓治療治外,特定族群患者建議使用可以降低心臟與腎臟風險的藥物。
動脈粥樣硬化性心血管疾病 (atherosclerotic cardiovascular disease, ASCVD)、高風險患者
ASCVD每個實驗定義不同,通常包含心肌梗塞 (myocardial infarction, MI)、腦中風 (stroke)或經過血管重建手術 (revascularization),其餘隨研究不同的定義包含暫時腦缺血 (transient ischemia attack, TIA)、不穩定心絞痛 (unstable angina, UA)、截肢 (amputation)、冠狀動脈疾病 (coronary artery disease, CAD)。
高風險患者每個實驗定義不同,通常為55歲以上合併兩種以上危險因子,包括肥胖、高血壓、抽菸、高血脂和蛋白尿。
以上患者建議使用有心血管實證根據的GLP-1RA或SGLT2i。若HbA1c未達標,可以併用GLP-1RA和SGLT2i,也可以使用低劑量Thiazolidinedione (TZD)。
心衰竭 (heart failure, HF)患者
有症狀的心臟衰竭,不論是低收縮分率心臟衰竭 (heart failure with reduced ejection fraction, HFrEF)或保留收縮分率心臟衰竭 (heart failure with preserved ejection fraction, HFpEF),皆建議使用在心血管實證和腎臟實證有根據的SGLT2i。
慢性腎臟病 (chronic kidney disease, CKD)
慢性腎臟病定義為腎絲球過濾率 (estimated Glomerular filtration rate, eGFR) <60 ml/min/1.73m2或是白蛋白尿 (albuminuria) ≥ 30毫克/dL。
以上患者建議使用有腎病變預後實證的SGLT2i,例如Canagliflozin、Dapagliflozin和Empagliflozin,eGFR ≥20 ml/min/1.73m2可以使用直到透析為止。
若SGLT2i無法耐受或禁忌使用,可以使用有心血管實證根據的GLP-1RA。若HbA1c未達標,可以併用GLP-1RA和SGLT2i。
第二型糖尿病治療目標2:血糖體重達標維持
除了在高風險病患使用可降低心臟、腎臟風險的SGLT2i與GLP-1RA,糖尿病治療目標需要血糖與體重同樣達標與維持。
血糖達標
選擇效果好的藥物,包括Metformin或複方藥物有效達標並維持,並且避免低血糖風險。
降血糖效果超高的藥物:Dulaglutide(高劑量)/Semaglutide/Tirzepatide、胰島素Insulin、口服複方藥物/混注型(GLP-1RA/Insulin)。
降血糖效果高的藥物:上述以外GLP-1RA、Metformin、SGLT2i、Sulfonylurea (SU)、TZD。
降血糖效果中等的藥物:雙基胜肽酶抑制劑 (Dipeptidyl peptidase 4 inhibitors, DPP4i)
體重達標
除了營養調整、飲食習慣改變、運動之外,也考慮使用藥物治療,在極度肥胖患者也考慮減重手術。
降體重效果超高的藥物:Semaglutide、Tirzepatide。
降體重效果高的藥物:Dulaglutide、Liraglutide。
降體重效果中等的藥物:上述以外GLP-1RA、SGLT2i。
無降體重效果藥物:DPP4i、Metformin。
藥物種類與分析
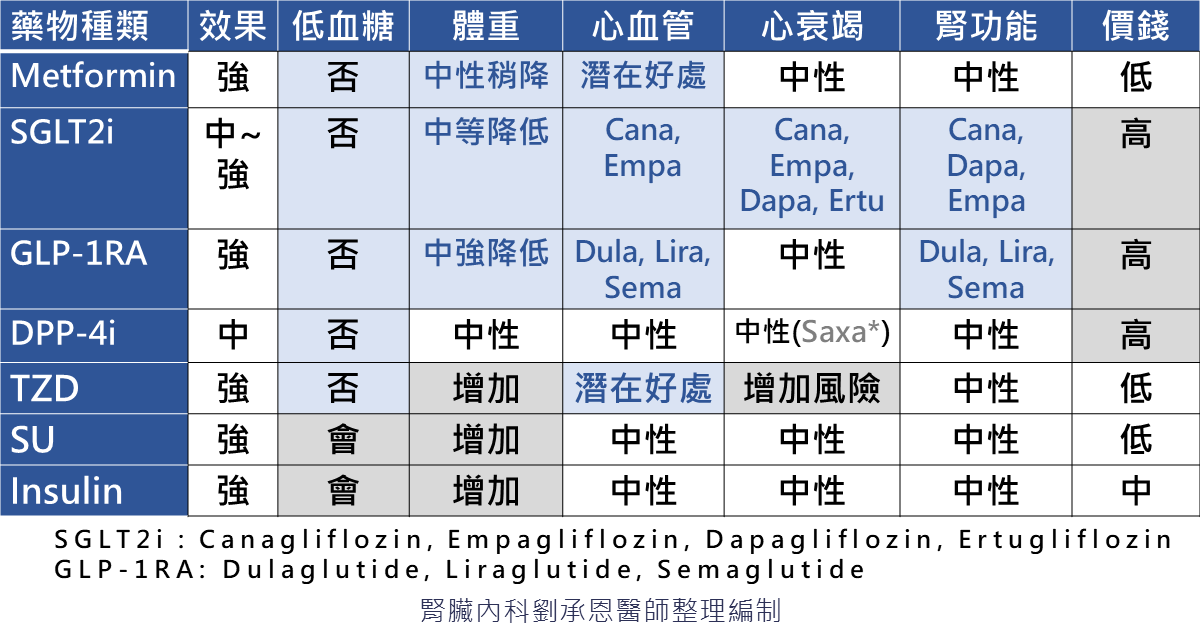
藥物選擇需考量效果、低血糖風險、價錢,以及對體重、心血管、心衰竭與腎臟功能的影響。
Metformin
eGFR小於30ml/min/1.73m2為使用禁忌,須注意腸胃道副作用,可從低劑量開始往上調整或使用長效型配方。可能造成維生素B12缺乏。
SGLT2i
在心血管、心衰竭、腎臟預後實證上表現優異,須注意eGFR較低會減低降糖效果。SGLT2i常見副作用是生殖泌尿道感染,使用時也需要注意體液容積不足風險。SGLT2i極少造成酮酸中毒 (diabetic ketoacidosis, DKA),當發生酮酸中毒時血糖可能正常,建議手術前3~4天、重症虛弱、長時間禁食期間避免使用。
GLP-1RA
最常見腸胃道副作用,建議從低劑量開始,慢慢往上調整來降低副作用。 在動物實驗中發現增加甲狀腺腫瘤風險,人類目前沒發現但仍需小心使用。
DPP4i
Saxagliptin可能增加心臟衰竭風險。胰臟炎、關節疼痛等少見。
TZD
會增加體液滯留造成水腫、體重增加,也增加心臟衰竭風險 (pioglitazone, rosiglitazone)。增加骨折風險。
SU、Insulin
效果好,但低血糖風險高!
針劑藥物使用流程
建議GLP-1RA或GIP/GLP-1RA優先於Insulin使用,其後加上基礎胰島素Basal Insulin(避免超過0.5U/kg/天)。若無法達標加上餐前胰島素Prandial Insulin (最大餐開始→2~3餐皆注射)。最後考慮合併基礎胰島素和餐前胰島素,或是混注型胰島素Premixed Insulin(每天1~3次)使用。